進化の要因である突然変異はどのようにして生じるのでしょうか?塩基配列が変わってしまうげんいんとしては大きく2つのことが考えられます。1つは、細胞が分裂する際のDNA複製エラーです。もう一つが、放射線や化学物質によるDNA変異です。どちらの貢献度が大きいのでしょうか。生成AIに訊いてみたところ、回答はバラバラでした。よって、一つの答えを鵜呑みにするのは危険です。
まずchatGPTに訊いてみます。
In evolution, mutations in germ cells caused by chemical or physical mutagens generally have a larger contribution to long-term evolutionary change compared to errors during DNA synthesis.
Here’s why:
- Germline vs. Somatic Impact:
- Errors during DNA synthesis (replication errors) happen frequently in both somatic and germ cells. However, errors in somatic cells do not contribute to evolution, as they are not passed on to offspring.
- Mutations in germ cells, induced by external factors (chemical mutagens, radiation, etc.), directly affect the genetic material that is inherited by the next generation, making them more significant in evolutionary terms.
- Mutation Frequency:
- Although DNA synthesis errors are common, most are corrected by proofreading and repair mechanisms. The remaining errors often result in minor variations.
- Mutagens, on the other hand, can cause more substantial and diverse changes in DNA, increasing the likelihood of significant phenotypic changes that drive evolutionary processes.
- Environmental Factors:
- External factors (like UV radiation or chemical exposure) that cause germline mutations can introduce new traits or enhance genetic diversity, providing material for natural selection to act upon. This can lead to adaptive evolution over generations.
- Evolutionary Novelty:
- Large-scale evolutionary shifts, such as those leading to speciation or major morphological changes, are often associated with environmental mutagens, which can cause larger genetic rearrangements (e.g., chromosomal mutations, large deletions, or duplications).
However:
- DNA synthesis errors still play a role, especially in generating small-scale genetic variations that accumulate over time (known as genetic drift or neutral mutations).
- The relative contribution can vary depending on the evolutionary timescale and environmental pressures.
In summary, while both mechanisms contribute to genetic variation, mutations in germ cells by chemical or physical mutagens tend to have a greater and more lasting impact on evolution.
1. Germline vs. Somatic Impact:
- DNA Replication Errors: Errors during DNA replication can occur in both somatic and germ cells. However, only mutations in germ cells are heritable and can be passed to offspring, influencing evolutionary processes. Somatic mutations, while potentially leading to diseases like cancer within an individual, do not contribute to evolution as they are not inherited.
- Mutations in Germ Cells by Mutagens: Mutations induced by chemical or physical mutagens in germ cells directly alter the genetic information passed to the next generation, thereby playing a significant role in evolution. Environmental mutagens can cause DNA damage leading to mutations if not properly repaired.
2. Mutation Frequency:
- DNA Replication Errors: The DNA replication machinery has high fidelity, with error rates as low as 1 mistake per 10–100 million nucleotides, thanks to proofreading and repair mechanisms. Despite this, replication errors do contribute to genetic variation.
- Mutagens: Exposure to chemical and physical mutagens can significantly increase mutation rates by causing DNA damage that, if not accurately repaired, leads to mutations. For instance, UV radiation can induce pyrimidine dimers, leading to errors during DNA replication.
3. Environmental Factors:
- Mutagens and Evolution: Environmental mutagens, such as radiation and chemicals, can induce mutations in germ cells, introducing new genetic variations into a population. These variations are essential for natural selection and adaptive evolution. For example, oxidative DNA damage is a common result of environmental factors and can lead to mutations if not properly repaired.
4. Evolutionary Novelty:
- Large-Scale Mutations: Mutagens can cause significant genetic alterations, such as insertions, deletions, or chromosomal rearrangements, leading to substantial phenotypic changes. These large-scale mutations can be pivotal in the development of new traits and may drive speciation events. For instance, replication slippage, a form of mutation, can lead to expansions or contractions in DNA sequences, contributing to genetic diversity.
Conclusion:
While both DNA replication errors and mutagen-induced mutations contribute to genetic variation, the latter, especially when occurring in germ cells, often have a more profound impact on evolutionary processes due to their potential to introduce significant genetic changes and their direct transmission to offspring.
根拠がウィキペディアだったりするので、いまいちですね。
consensus.appに訊いたら真逆の回答でした。
In the context of evolution, both errors during DNA synthesis and mutations in germ cells caused by chemical or physical mutagens contribute to mutagenesis. However, errors during DNA synthesis, particularly during DNA replication, are often highlighted as a significant source of mutations.
Errors During DNA Synthesis
- DNA Replication Errors: Most mutations in actively dividing cells originate during DNA replication. Errors can occur when copying an undamaged DNA template or during the bypass of DNA lesions, making DNA replication a major contributor to mutagenesis1 3 6.
- Error-Prone DNA Polymerases: DNA polymerases, especially those involved in translesion synthesis, can introduce mutations by misincorporating incorrect nucleotides or through frameshift deletions, contributing significantly to mutagenesis2 9.
- Repair-Associated Mutations: DNA repair processes, such as homologous recombination and non-homologous end-joining, can also introduce mutations, particularly when repairing double-strand breaks1 10.
Mutations in Germ Cells by Chemical or Physical Mutagens
- Environmental Mutagens: Chemical and physical mutagens can cause DNA lesions that lead to mutations if not properly repaired. These mutagens include alkylating agents and radiation, which can induce various types of DNA damage2 5 8.
- Germ Cell Mutagenesis: Studies on germ cells, particularly in model organisms like mice, have shown that chemical and radiation-induced mutations can vary significantly depending on the germ cell stage and the type of mutagen8.
Conclusion
While both mechanisms contribute to mutagenesis, errors during DNA synthesis, particularly those occurring during replication and repair processes, are often emphasized as a primary source of mutations. Chemical and physical mutagens also play a crucial role, especially in germ cells, but the inherent errors in DNA replication and repair processes are consistently highlighted as significant contributors to evolutionary mutagenesis.
1 Mutagenesis and the three R’s in yeast. Mutagenesis in yeast occurs through DNA replication, recombination, and repair processes, with recombination and repair contributing more to mutagenesis than previously thought. 2006·14Citations·Amy L. Abdulovic et al.· DNA repair
2 Mechanisms of mutagenesis induced by DNA lesions: multiple factors affect mutations in translesion DNA synthesis Multiple factors, including DNA lesions, affect mutations in translesion DNA synthesis, including misincorporation of incorrect nucleotides, frameshift deletions, and blockage of DNA replication. 2020·8Citations·Huidong Zhang· Critical Reviews in Biochemistry and Molecular Biology
3 Error-prone bypass of DNA lesions during lagging strand replication is a common source of germline and cancer mutations Error-prone damage bypass on the lagging strand plays a major role in human germline and cancer mutations, with at least 10% of mutations arising due to DNA damage. Info In Vitro Trial Info Rigorous Journal 2017·33Citations·V. Seplyarskiy et al.· Nature genetics
4 Protection of the C. elegans germ cell genome depends on diverse DNA repair pathways during normal proliferation Different DNA repair pathways contribute to preventing germ cell mutagenesis, with a broad spectrum of mutational outcomes observed in C. elegans germ cells. Info Rigorous Journal Ask this paper 2021·17Citations·B. Meier et al.· PLoS ONE
5 Mutational signatures are jointly shaped by DNA damage and repair Combining exposure to DNA damaging agents and DNA repair deficiency in C. elegans leads to altered mutation rates and new mutational signatures. Info Highly Cited 2019·144Citations·Nadezda V. Volkova et al.· Nature Communications
6 The biochemistry of mutagenesis. Mutagenesis, a process that causes genetic changes, can lead to metabolic and neoplastic diseases, and its mechanisms are subject to genetic controls. Info Highly Cited 1976·347Citations·J. Drake et al.· Annual review of biochemistry
7 POLE proofreading defects: Contributions to mutagenesis and cancer. Mutations in DNA polymerases contribute to mutagenesis and tumor development, particularly in cancers involving DNA polymerase epsilon. 2019·47Citations·Vivian S. Park et al.· DNA repair
8 Role of mouse germ‐cell mutagenesis in understanding genetic risk and in generating mutations that are prime tools for studies in modern biology Mouse germ-cell mutagenesis has played a crucial role in assessing genetic harm from radiation and chemicals, and its products have contributed to modern biology by providing valuable tools for studying various aspects of biology. 1994·14Citations·L. B. Russell· Environmental and Molecular Mutagenesis
9 Unravelling roles of error-prone DNA polymerases in shaping cancer genomes Error-prone DNA polymerases may compensate for DNA repair defects, shaping the mutational landscape of cancer cells. Info Rigorous Journal 2021·0Citations·Cyrus Vaziri et al.· Oncogene
10 Mutations arising during repair of chromosome breaks. https://www.annualreviews.org/content/journals/10.1146/annurev-genet-110711-155547 Homologous recombination, a safe pathway for repairing double-strand chromosomal breaks, is a significant source of mutations that contribute to human disease and evolution.
consensusの回答もイマイチでした。進化の原動力としての突然変異について訊いたのに、単に突然変異のことしか根拠となる論文がありません。10個挙げられた論文のうち10番目だけ進化に言及があるようです。要旨に”Overall, homologous recombination, which is traditionally considered a safe pathway of DSB repair, is an important source of mutagenesis that may contribute to human disease and evolution.”とあります。しかしconsensusの要約だと、論文の要旨には存在していたmayが抜けてしまって断定的に書き直されています。これは全く信用なりません。AIはまだまだ信頼できないですね。
自分がした質問ではないのですが、同時に表示されていたすでにあった質問に対する答えをみると、こっちのほうが進化に関連した論文を引用した答えになっていました。並列して要因の候補を回答していて、どれの貢献が特に大きいという言い方はしていません。
The main sources of DNA mutations in evolution include spontaneous mutations, transposable elements, replication errors, and quantum effects. These mutations are crucial for generating genetic variation, which is essential for evolutionary processes.
Key Sources of DNA Mutations
-
Spontaneous Mutations: These are random mutations that occur naturally and are the ultimate source of genetic variation necessary for evolution. They can arise from errors during DNA replication or from environmental factors6 8.
-
Transposable Elements: These mobile DNA sequences can cause mutations by inserting themselves into new genomic locations. They are a significant source of spontaneous mutations and can have dramatic effects on organismic evolution2 4.
-
Replication Errors: DNA replication errors are a common source of mutations. The fidelity of DNA replication is crucial, and errors that escape repair mechanisms, such as DNA mismatch repair, can lead to mutations. These errors are often corrected by cellular repair systems, but deficiencies in these systems can increase mutation rates7.
-
Quantum Effects: Quantum mechanics, particularly quantum tunneling, has been proposed as a mechanism that can lead to genetic mutations. This suggests that quantum effects might play a role in the mutation process, contributing to evolutionary changes3.
-
Microsatellite Mutations: These are mutations in repetitive DNA sequences that occur at higher rates than other types of DNA. They contribute to genetic variation and are influenced by factors such as age, sex, and the specific genomic context9.
Conclusion
DNA mutations arise from a variety of sources, including spontaneous mutations, transposable elements, replication errors, and quantum effects. These mutations are essential for creating the genetic diversity upon which natural selection acts, driving evolutionary change. Understanding these sources helps elucidate the mechanisms of evolution and the development of genetic variation.
1 Evolution of the Insertion-Deletion Mutation Rate Across the Tree of Life An inverse relationship exists between mutation rate and effective population size, suggesting that natural selection reduces mutation rates per effective genome until random genetic drift becomes overwhelming. Info Highly Cited 2016·89Citations·Way Sung et al.· G3: Genes|Genomes|Genetics
2 Transposable elements: possible catalysts of organismic evolution. Transposable elements are a major source of spontaneous mutations, and their potential to produce mutations with dramatic effects on organismic evolution is discussed. Info Highly Cited 1995·134Citations·John F. McDonald· Trends in ecology & evolution
3 Quantum Evolution and Genetic Mutations Quantum tunnelling plays a main role in genetic mutation, which is the origin of evolution in organisms. Ask this paper 2024·0Citations·H. Hossieni· Qeios
4 Evolutionary Genetics: Mobile DNAs as Sources of Adaptive Change? Mobile DNA insertions in Drosophila simulans are associated with an apparent selective sweep and an elevation in expression level of an adjacent gene, creating insecticide resistance. 2004·16Citations·J. Brookfield· Current Biology
5 Genetic drift, selection and the evolution of the mutation rate Natural selection primarily improves DNA-replication fidelity, with random genetic drift setting the ultimate limits to what can be achieved. Info Highly Cited 2016·641Citations·M. Lynch et al.· Nature Reviews Genetics
6 Evolutionary tuning knobs Simple sequence repeats (SSRs) provide a source of abundant quantitative genetic variation and may serve as ‘tuning knobs’ for efficient adaptation in evolution. Info Highly Cited 1997·156Citations·D. King et al.· Endeavour
7 DNA mismatch repair preferentially protects genes from mutation MMR deficiency increases the frequency of smaller-scale insertions and deletions, and preferentially protects genes from mutation, impacting understanding of genome evolution during natural selection and human tumor growth. Ask this paper 2018·64Citations·E. Belfield et al.· Genome Research
8 Genomes and the origin of genetic variation Selfish genetic elements and unequal crossing over are main sources of DNA mutations in evolution, contributing to the presence of large amounts of noncoding DNA and the repetitive structure of the genome. 2019·0Citations·Glenn-Peter Sætre et al.· Evolutionary Genetics
9 Microsatellite mutations in the germline: implications for evolutionary inference. Microsatellite mutation rates in the germline are highly heterogeneous, with differences between species, repeat types, loci, and alleles, and age and sex affecting the mutation rate. Info Highly Cited 2000·724Citations·H. Ellegren· Trends in genetics : TIG
10 The origins, determinants, and consequences of human mutations Recent insights into the rates, spectrum, and determinants of genomic mutations inform our understanding of both Mendelian and complex human diseases, and future research should focus on developing new technologies to access and quantify mutations. Info Highly Cited 2015·142Citations·J. Shendure et al.· Science
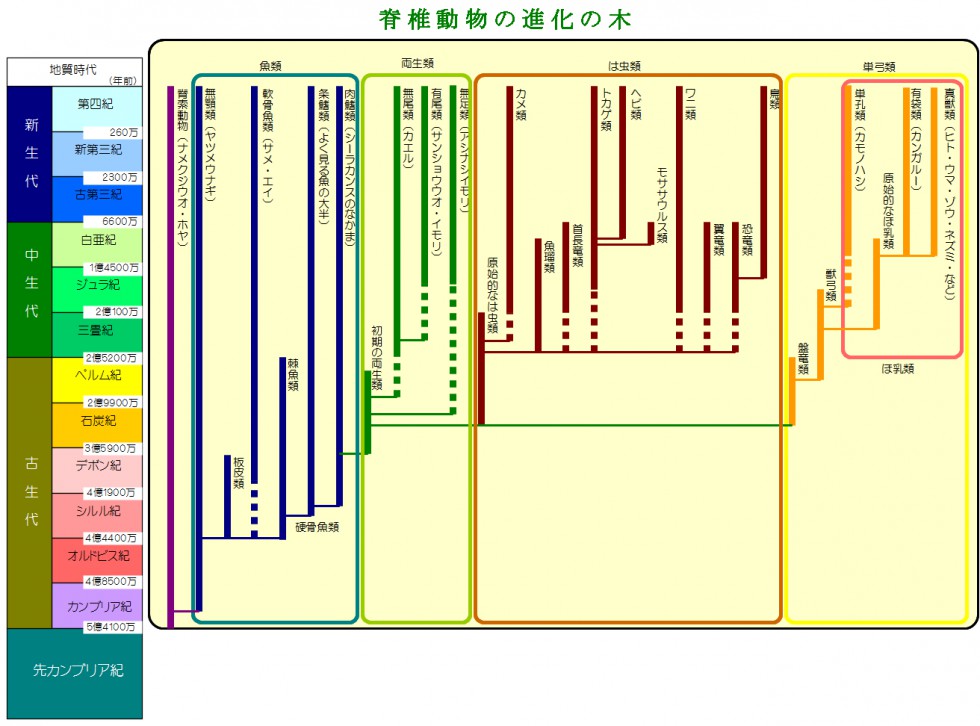 脊椎動物の進化 熊本県博物館ネットワークセンター
脊椎動物の進化 熊本県博物館ネットワークセンター
