口や鼻から吸い込んだ空気は気管を通って、その先の気管支(名前が変わっただけ)に入り、気管支の枝分かれを経て、肺胞に到達します。気管は体の中心にあるまっすぐな部分で、分岐した先からは「気管支」と呼ばれるようになるのだそうです。気管支の分岐の数は一番多いところで23回にもおよぶそう。そして、先端部にある肺胞の数は左右の肺をあわせると10億個に上るのだそうです。下のNHKのリンク先では動画で、は、気管内視鏡が気管支の中に入っていく様子が示されています。さすがNHKが子供向けにつくった動画だけあって、とてもわかりやすい。
- ヒトの呼吸器のしくみ NHK for School
下のYOUTUBEの動画でも、気管内視鏡で気管支の内部を検査している様子が映し出されています。模式図などで気管支が枝わかれしているのは頭では理解できますが、こうやって内視鏡を中にいれて実際に分岐部に遭遇すると枝分かれが「実感」できます。
【聖マリアンナ医科大学病院】気管支鏡検査と肺癌診療の進歩 呼吸器内科森川 慶 聖マリアンナ医科大学病院 メディカルサポートセンター チャンネル登録者数 258人
声帯
声帯腫れテスト:声帯損傷を簡単にチェック Fauquier ENT チャンネル登録者数 61.8万人
肺の発生
- 腺様期 pseudoglandular period
- 管状期 canalicular period
- 終末嚢期 terminal sac period
- 肺胞期 alveolar period
参考サイト
- 「呼吸器系」ユニット (Respiratory System) 呼吸器系の講義計画表・講義録 https://www.lab2.toho-u.ac.jp/med/physi1/respi.html 大学の発生学の講義録でとても分かりやすい説明です。
- https://embryology.ch/en/organogenesis/respiration-tract/phases-of-lung-development/introduction.html
- Introduction – Lung Development by John McLachlan, PhD Lecturio.com
- Histological Differentiation – Lung Development by John McLachlan, PhD Lecturio.com LECTURIOの講義動画ではいろいろな教科書から挿絵が借用されていますが、この動画ではカールソン Carlsonの教科書の図が多用されていました。なので、Carlsonの教科書を読みながらこの動画を視聴したり、逆にこの動画を見たあとでカールソンの教科書を読み直したりすると効果的に勉強できます。
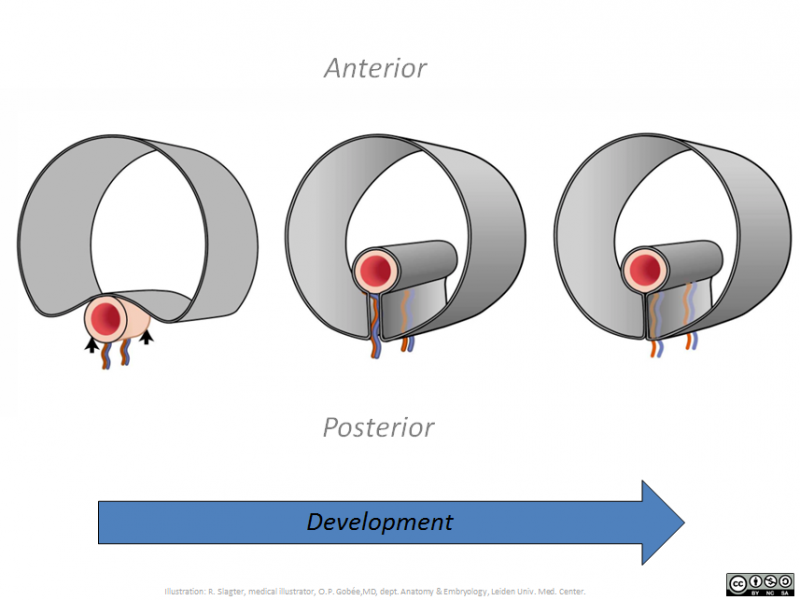
- Transverse View – Lung Development by John McLachlan, PhD Lecturio.com 胎児は生まれるまえに「呼吸」をしており羊水を肺に吸い込んでいるそうです。しかし生まれてきて最初の呼吸をしたあとは、肺の中に残っている液体は肺胞で毛細血管に吸収されて、問題は生じないようです。
- Respiratory Distress Syndrome – Lung Development by John McLachlan, PhD Lecturio.com
- Tracheo-esophageal Fistulas – Lung Development by John McLachlan, PhD Lecturio.com
腸管から気管が分化するときのシグナル
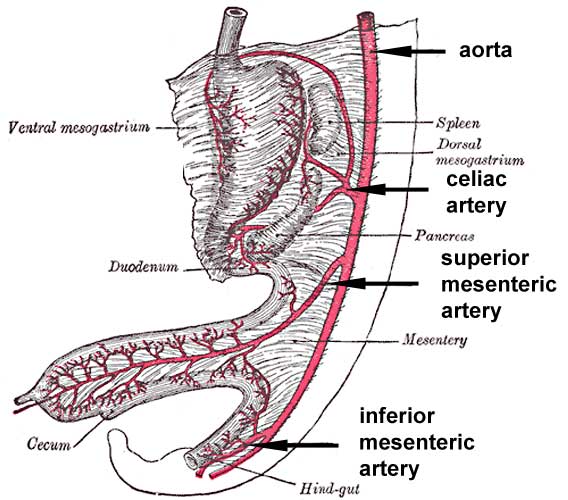
肺は消化管から芽を出すことで作られます。
Fig. 1. Overview of the stages of lung development. Lung endoderm specification begins at ∼E9.0 on the ventral side of the anterior foregut endoderm (yellow) where initiation of Nkx2.1 expression commences. https://europepmc.org/article/pmc/pmc3899811
気管の分岐の分子シグナル
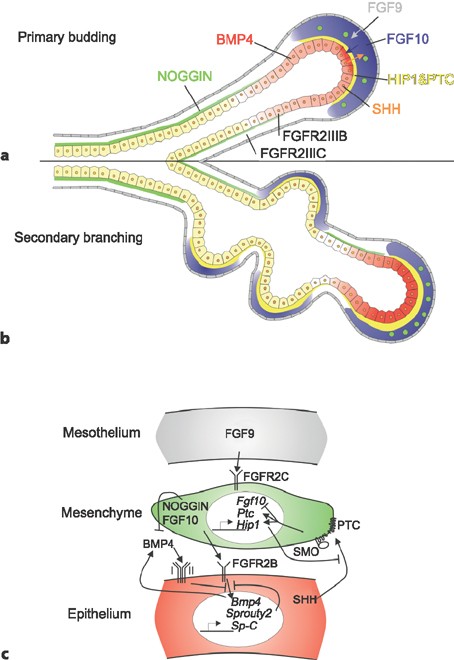
Specification and early development of the lung endoderm. (A) The lung endoderm (marked by Nkx2.1 expression, blue) is first specified on the ventral side of the anterior foregut at E9.0. Wnt2/2b and Bmp4 signaling (indicated in orange???) from the surrounding mesoderm is required for this specification and for patterning of the anterior foregut in a ventral-dorsal manner. Wnt2 and Wnt2b signal via β-catenin to promote the expression of Nkx2.1 whereas Bmp4 represses the inhibitory action of Sox2 on Nkx2.1 expression. (B) During lung development, Fgf10 is essential for branching morphogenesis and is expressed in the mesenchyme surrounding developing branch points (Fgf10 expression indicated in green). This expression is restricted by epithelial expression of genes such Shh and Bmp4 (purple). Fgf10 also directs the orientation of epithelial cell division through regulation of Ras/Sprouty, setting up the appropriate direction of branch growth. https://europepmc.org/article/pmc/pmc3899811
FGF-Regulated ETV Transcription Factors Control FGF-SHH Feedback Loop in Lung Branching Developmental Cell Volume 35, Issue 3, 9 November 2015, Pages 322-332 Journal home page for Developmental Cell Article https://www.sciencedirect.com/science/article/pii/S153458071500653X
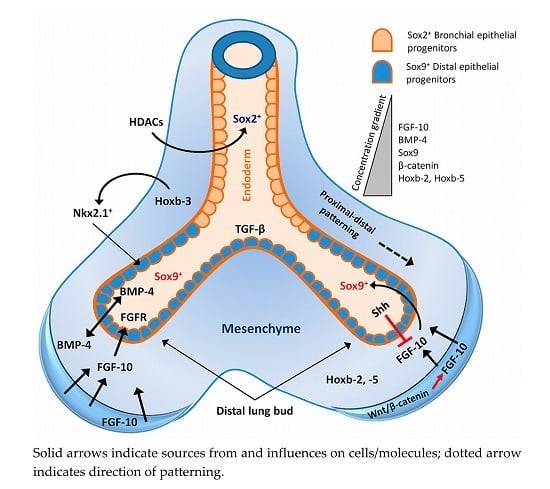
Figure 1. Epithelial-mesenchymal cross-talk and governing signalling during early development and branching morphogenesis of lung. Factors are represented only at sites where the expression is most abundant. Fibroblast growth factor-10 (FGF-10) is highly expressed in the distal mesenchyme and acts as a chemotactic focus for the epithelium during lung budding. FGF-10 also regulates Sox9 expression in the distal epithelial progenitors and induces bone morphogenetic protein (BMP)-4 expression. Sox2 expression in the proximal epithelium is under regulation of histone deacetylases 1/2 (HDAC1/2) signalling. FGF-10 expression in the mesenchyme is regulated by Wnt/β-catenin signalling (red arrow). A high concentration of BMP-4 signal also serves to locally inhibit endoderm proliferation, thereby inducing the lateral outgrowth of new airway branches. Sonic hedgehog (Shh) at the distal tips functions to downregulate FGF-10 expression in the mesenchyme, which limits local budding. Transforming growth factor-β (TGF-β) signalling also prevents local budding, by decreasing endodermal proliferation and by stimulating synthesis of matrix components at branch points. Solid arrows indicate sources from and influences on cells/molecules; dotted arrow indicates direction of patterning.
https://www.mdpi.com/1422-0067/17/1/128
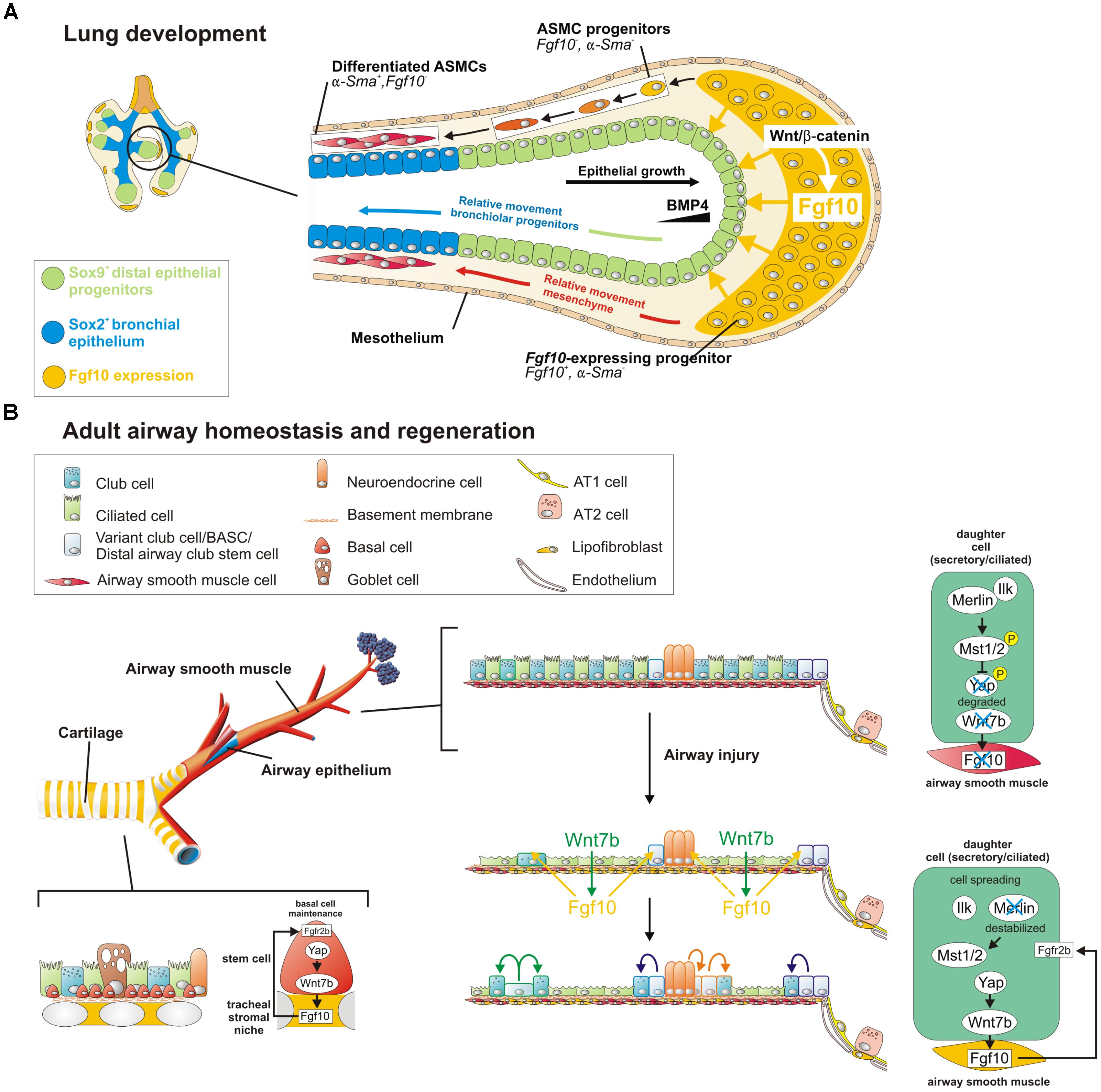
FIGURE 1. A Wnt7b-Fgf10 epithelial-mesenchymal crosstalk maintains distal epithelial progenitors during lung development and becomes reactivated in the adult lung to regenerate injured airway epithelium. (A) During the branching stage of lung development, Fgf10 is expressed by mesenchymal progenitor cells, which depends on Wnt/β-catenin signaling, and acts on the distal epithelium to induce Bmp4 and Sox9 expression to keep them in an undifferentiated state. As the epithelial tube grows toward the Fgf10 source, Sox9 + progenitors acquire more proximal positions, switch on Sox2 expression and acquire bronchial epithelial fate. Simultaneously, distal Fgf10-expressing airway smooth muscle (ASMC) progenitors encounter epithelial Bmp4 and Shh (not shown) causing them to stop expressing Fgf10 and differentiate into mature ASMCs as they relocate proximally.
Fgf10 Signaling in Lung Development, Homeostasis, Disease, and Repair After Injury MINI REVIEW article Front. Genet., 25 September 2018 Sec. Stem Cell Research Volume 9 – 2018 | https://doi.org/10.3389/fgene.2018.00418 https://www.frontiersin.org/journals/genetics/articles/10.3389/fgene.2018.00418/full
https://link.springer.com/referenceworkentry/10.1007/3-540-29623-9_3330
肺の分化のステージ
ヒトの肺の発生段階は5つであり肺芽期、腺様期、管状期、嚢状期、肺胞期に分類される http://www.hs-kyoto.net/?page_id=7544
I型肺胞上皮細胞
肺胞を構成する細胞の種類の中にI型肺胞上皮細胞(AT1細胞)と、II型肺胞上皮細胞(AT2細胞)とがあります。I型は肺胞を構成する主要な細胞です。肺胞の内部の空気の部分と、肺胞を取り囲む毛細血管の中の血液との間で酸素や二酸化炭素のやり取りを効率よく行うため、肺胞の壁をつくっているI型肺胞上皮細胞の厚みは非常に薄いものになっています。肺の肺胞の総表面積は約 70~100 m²(テニスコートほどの広さ)といわれており、その大部分がAT1細胞によって覆われています。
AT1 cells cover 95% of the gas exchange surface and are 0.1 µm thick to allow passive diffusion of oxygen into the blood stream. https://www.pnas.org/doi/full/10.1073/pnas.1906663116
出生時の変化
動脈管の閉鎖
- 胎児の動脈管では中膜の平滑筋細胞が円周方向,縦方向,らせん方向とさまざまな方向に配列し,ほかの血管と異なり,大きく収縮したり,拡張したりすることが可能である.
- 出生時の酸素分圧の上昇は動脈管の平滑筋細胞へのCaイオンの流入を促進し,動脈管収縮を一気に引き起こす.
- 平滑筋の収縮により機能的閉鎖し,内管が完全に閉鎖した動脈管は,中膜組織の低酸素状態をきたし,次第にアポトーシスによる動脈管壁の線維化と変性が生じて永久的な閉鎖となる.
https://www.jstage.jst.go.jp/article/shinzo/46/2/46_166/_pdf/-char/ja