本来は雇用の安定を目的とした「労働契約法18条1項に基づく」無期雇用への転換ですが、それがむしろあだとなって、無期転換の権利が得られる直前に雇用の継続を打ち切られる、いわゆる「雇止め」がアカデミアの世界で当たり前に起こっています。大学事務の場合「5年」を過ぎると無期転換の権利が得られます。任期付き教員には、「労働契約法18条1項の特例である大学の教員の任期に関する法律7条1項」が適用され、無期転換の権利が得られるまでの年数は「5年」でなく「10年」になっています。研究者も同様に「科学技術・イノベーション創出の活性化に関する法律」によって、労働契約法で定めた5年ではなく10年とされています。
事務職員でも、教員でも、研究者でも、要するに無期転換の権利が発生する前に、クビを切られる(雇用契約の更新を行わない)ということが起こるのです。それが「雇止め」です。ただし、雇止めと言う言葉は、研究者や研究職の教員に対しては使われることはなくて、単に任期切れという言い方をするのが普通だと思っていたのですが、新聞記事を見ると、雇止めという言葉は研究者やPIに関しても使われていました。多くの研究者は任期が切れる前に次の職を探すという考え方をしているため、「雇止めされた」というよりも「任期が切れた」と認識していると思います。ずっと働けると期待していた場合に「雇止めされた」という感情が湧くのでしょう。気持ちがどうであれ、実態は同じです。
下の弁護士ドットコムの解説が非常にわかりやすくまとまっています。
- 改正労働契約法18条1項:同法が施行された2013年4月以降に結ばれた契約を起算点として、契約期間が通算5年を超えると無期転換申込権が発生。
- 労働者による無期転換の申し込みを使用者は断ることができない
- 改正労働契約法の例外として「大学教員任期法」(大学の教員等の任期に関する法律) 「労働契約法の特例」として、有期雇用の大学教員については、無期転換申込権が発生するまでの期間を「5年」ではなく「10年」(同法7条)。「10年」を適用するには「多様な人材の確保が特に求められる教育研究組織の職に就けるとき」条件(同法4条)。具体的には「先端的、学際的又は総合的な教育研究であること」
- 労働契約法の例外として、「科技イノベ活性化法」(科学技術・イノベーション創出の活性化に関する法律)では、研究者についても同じく“10年特例”を適用することを定めている。
「ベテラン教員の雇止め」大学で相次ぐ…約20年勤務も無情通告、「無期転換」はできないのか? 2024年06月14日 10時26分 弁護士ドットコムニュース https://www.bengo4.com/c_5/n_17651/
下のブログ記事もとても分かりやすい。
- 研究者の雇い止め問題をいちから解説 2025年1月27日 アカデミアノート
もともと有期であるということが雇用契約書に書かれていたのに、なぜ無期転換を期待するのか?に関して、自分も正直よくわからないところがあります。裁判でいったい何が論点、争点になるのでしょうか?下の解説を読んでなるほどと思いました。
雇止めが無効になるためには,労働契約法19条の要件を満たす必要があります。すなわち,第1の要件として,有期労働契約が更新されるものと期待することについて合理的な理由があること。第1の要件が満たされれば,第2の要件として,雇止めに客観的合理的理由がなく,社会通念上相当でない場合に,雇止めが無効になるのです。
大学の准教授に対する雇止め事件2020年1月8日 金沢合同法律事務所 https://kanazawagoudoulaw.com/tokuda_blog/202001088941.html
法律の改正が2013年だったため、5年後に無期転換できるかどうかという大問題が表面化したのは2018年でした。
- 国立大で多数の雇止め… 国立大で多数の雇止め問題 : 違法・脱法行為許さない運動が全国に拡大 (特集 どうする2018年問題) 雑誌 月刊労働組合 巻号 647号 2018年3月 記事 https://ndlsearch.ndl.go.jp/books/R000000004-I028879471 本文なし
事務系の場合が5年で、研究などの専門職の場合は10年後に無期転換の権利を得るので、2023年が、研究従事者にとっての正念場となりました。
研究者の雇止め問題は、研究者は流動的であるべきという考え方と、研究者にも普通の人間的な生活をする権利があるという考え方の2つが、せめぎあっているように思います。いつまでも短期契約を繰り返すだけだと、住む場所も一定しませんので、結婚して子供をもうけて安定した家庭をもつことが非常に難しくなります。実際、研究者同士が結婚した場合、夫婦がそれぞれの職を優先した結果ずっと別居している例が複数見られます。やはり研究者といえどもずっと流動的な環境を強いられるのは大変すぎます。
多くの研究プロジェクトが、時限付きの予算配分に依っているは、雇止めを生じさせている大きな要因です。人材の雇用財源が切れるのですから、それ以降の雇用はないわけです。最初からそれが分かっていてその職についたのに、なぜ無期雇用を要求できるのか?という論理がそこにあります。一番の問題は、有期雇用の職に就いていた人が、業績を挙げることにより無期雇用の職に就いてしかるべきなのに、そのような無期雇用の職が今の日本のアカデミアの中にはほとんど存在しないことです。そのため、いつまでも有期雇用の職を転々とするはめになってしまいます。教授や独立准教授といったPI(研究室主宰者)の職は、数十倍~数百倍の競争率であり、ほとんどの人はあぶれてしまいます。
理研の雇止め問題
2022 年 9 月 30 日に、理研経営陣は理研ホーム ページとマスコミに対して「理研の新しい人事施 策について」を公表した。そこには「通算契約期 間の上限(5/10 年の雇用上限)撤廃」が明記さ れていたが、「通算契約期間の上限」の実際の撤 廃は 2023 年 4 月からであり、2023 年 3 月の雇止 めは強行された。https://www.cc.mie-u.ac.jp/~admin-law/25so-gaku/yoko/E1.pdf
- 科学論文なら“不合格”判決に原告が憤るわけ 理研雇い止め訴訟 垂水友里香 社会 環境・科学 速報 科学・テクノロジー 毎日新聞 2025/1/23 05:30 https://mainichi.jp/articles/20250120/k00/00m/040/100000c 男性は既に控訴しており、日本を代表する研究機関を相手取った裁判の審理は控訴審に移る。 2011年に採用された男性は、1年の有期雇用契約を10回更新しながら、10年以上にわたって研究を続けてきた。乳がんの早期検出や手術に用いるがん蛍光マーカーの技術で成果を出し、理研で研究室を主宰する部長職のチームリーダーとなっていた。‥ 理研は16年に就業規則を変更し、有期雇用に10年の上限を設け、その起算点を13年とした。男性は10年の期限を迎える直前の23年3月末に雇い止めされた。
- 理研、雇い止め対応変遷 事実上の「無期転換封じ」に訴訟相次ぐ 毎日新聞 2024/12/20 13:19(最終更新 12/20 19:17)理化学研究所(本部・埼玉県和光市)から違法な雇い止めをされたとして、生命科学系の男性研究者(64)が地位の確認を求めた訴訟で、さいたま地裁(鈴木尚久裁判長)は20日、原告側の請求を退けた。
- 理研の雇い止め問題で露見、研究者の流動性を支えてきた人事制度のもろさ 2023年06月25日 「10年の雇用上限による雇い止めは97人。チーム解散による雇い止めが87人。合計184人が雇い止めに遭った」。理研労働組合の金井保之執行委員長はこう説明する。2023年3月末に任期満了を迎える予定だった380人の48%が理研を去った。そのうち126人は大学や企業などの仕事に就いた。一方、理研は425人のポストを新設し、196人が理研で新しいプロジェクトを担っている。
- 理研、雇い止め批判の回避狙うカラクリの実態 3月末のリストラ強行へ、迫るタイムリミット 奥田 貫 : 東洋経済 2023/03/23 6:00 https://toyokeizai.net/articles/-/661179 理研を訴えている研究者らは、訴訟の中で「APが終わった後も無期転換への申込権を行使すれば、理研で研究を続けられるのか」の説明を求めているが、理研は否定的だ。
東北大学の雇止め問題
- 経営法曹 巻号 220号 2024年6月 記事 国立大学法人東北大学… 国立大学法人東北大学(雇止め)事件 仙台高裁令和5年1月25日判決 有期労働契約について、その雇止めが、無期労働契約における解雇と同視することができるといえるためには、当該有期労働契約が、契約期間の満了ごとに当然更新を重ねてあたかも無期労働契約と異ならない状態で存在していたといえることを要するとした1審判断が維持された例 (年間重要判例 年間重要判例検討会(第20回)報告 : 令和5年下期(7~12月)発行の裁判例集登載分) 国立大学法人東北大学(雇止め)事件 仙台高裁令和5年1月25日判決 有期労働契約について、その雇止めが、無期労働契約における解雇と同視することができるといえるためには、当該有期労働契約が、契約期間の満了ごとに当然更新を重ねてあたかも無期労働契約と異ならない状態で存在していたといえることを要するとした1審判断が維持された例 (年間重要判例 年間重要判例検討会(第20回)報告 : 令和5年下期(7~12月)発行の裁判例集登載分) 国立国会図書館請求記号 Z2-832 国立国会図書館書誌ID 033615946 https://ndlsearch.ndl.go.jp/books/R000000004-I033615946
その他の大学の雇止め問題(教育職)
羽衣国際大
大学教員が無期転換を得るのは一律10年というわけではなく、5年か10年間の判断が大学に委ねられるようです。下の裁判の事例は、教育職に就いていた大学教員が5年過ぎたから無期転換をお願いしたのに、あなたの職は例外が適用されるので5年ではなく10年ですよ、だから今10年が経過する前にあなたの雇用の契約更新を行わないことに違法性はないですよという大学側の主張が通ったという話。
- 第336号 大学教員の無期転換権行使の有効性 ~大学の教員等の任期に関する特例法の不適用判断を覆した最高裁判決の意義~ ~~学校法人羽衣学園(羽衣国際大学)事件 (最高裁第一小法廷令和6年10月31日判決)※1~~ 文献番号 2025WLJCC001 明治大学 教授 野川 忍 https://www.westlawjapan.com/column-law/2025/250107/
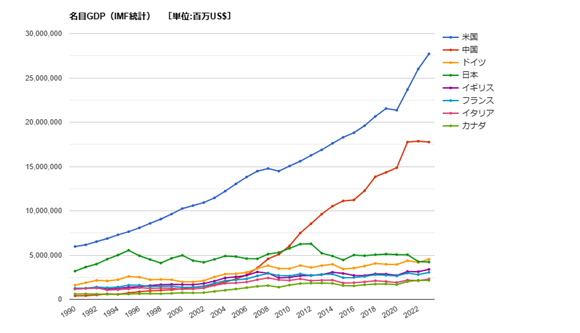 資料:GLOBAL NOTE 出典:IMF 【リンク先URL】 https://www.globalnote.jp/post-1409.html
資料:GLOBAL NOTE 出典:IMF 【リンク先URL】 https://www.globalnote.jp/post-1409.html.png)